研究テーマ
病態・生命機能解明のための機能性分子の創製
(i) 有機化学を基盤として、生体機能や病態の解明に挑むケミカルバイオロジー研究を通して、新規創薬ターゲットの探索や医薬品シーズの創出を目指す創薬研究
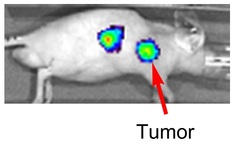
(ii) がんや生体内微量生理活性分子研究のためのイメージングプローブの開発と応用
スタッフ

奥田 健介 教授
担当科目:天然物化学・生物有機化学 医薬品開発 ロジカル思考演習Ⅰ・Ⅲ 基礎薬学演習 総合薬学講座 天然物化学・生薬学実習 アクティブ・ラボ 化学系創薬学特論(大学院)
学位:博士(薬学)
研究テーマ
医薬品シーズの創出および可視化小分子プローブの開発
所属学会
日本薬学会 日本がん分子標的治療学会 日本分子イメージング学会 国際癌治療増感研究協会 日本薬剤師会 アメリカ化学会 王立化学会(英国)
受賞歴
第17回国際癌治療増感研究協会 協会賞(2016年)

髙木 晃 講師
担当科目:薬学入門 天然物化学・生薬学実習 総合薬学講座 アクティブ・ラボ
学位:博士(薬学)
所属学会
日本薬学会 有機合成化学協会 国際癌治療増感研究協会
受賞歴
日本薬学会近畿支部奨励賞(平成28年度)
第24回国際癌治療増感研究協会 協会賞(2024年)
研究成果
最近の主な研究業績:詳しくは右上にリンクをはってある研究室オリジナルHPをご覧ください。
K. Usuguchi, A. Takagi, I. Takashima, K. Okuda; RSC Adv. 15(26), 20734–20744 (2025). "Elucidation of the acid reactivity of polyhedral orthoformates for the synthesis of carbasugar derivatives"
K. Okuda, A. Takagi, R. Shimizu, K. Nishi, N. Hayano, I. Takashima, M. Konishi; ChemMedChem, 2025, 20(7), e202400818. "Total Synthesis of Antiausterity Agent Callistrilone O Reveals Promising Antitumor Activity in a Melanoma Homograft Mouse Model"
A. Takagi, I. Takashima, K. Okuda; RSC Adv. 15(1), 428 (2025). “A turn-on fluorescent probe containing a β-ketoester moiety for the selective detection of intracellular hydrazine”
A. Takagi, K. Usuguchi, I. Takashima, K. Okuda; Chem. Pharm. Bull. 71(8), 641 (2023). “Development of 1,3,6-Tribenzoylated Glucose as an Antiausterity Agent Targeting Tumor Microenvironment”
K. Okuda, I. Takashima A. Takagi; J. Clin. Biochem. Nutr. 72(1), 1 (2023). “Advances in reaction-based synthetic fluorescent probes for studying the role of zinc and copper ions in living systems”
H. Matsumoto, S. Ando, E. Yoshimoto, T. Numano, N. Sultana, K. Fukamachi, M. Iinuma, K. Okuda, K. Kimura, M. Suzui; Oncol. Lett. 23(3), 99 (2022). “Extracts of Musa basjoo induce growth inhibition and changes in the protein expression of cell cycle control molecules in human colorectal cancer cell lines”
A. Takagi, K. Usuguchi, I. Takashima, K. Okuda; Org. Lett. 2021, 23(11), 4083 (2021). “Total Synthesis of Antiausterity Agent (±)-Uvaridacol L by Regioselective Axial Diacylation of a myo-Inositol Orthoester”
T. Sakai, Y. Matsuo, K. Okuda, K. Hirota, M. Tsuji, T. Hirayama, H. Nagasawa; Sci. Rep. 11, 4852 (2021). “Development of antitumor biguanides targeting energy metabolism and stress responses in the tumor microenvironment”
I. Takashima, Y. Inoue, N. Matsumoto, A. Takagi, K. Okuda; Chem. Commun. 2020, 56(87), 13327 (2020). “A fluorogenic probe using a catalytic reaction for the detection of trace intracellular zinc”
N. Goto, H. Hara, M. Kondo, N. Yasuda, T. Kamiya, K. Okuda, T. Adachi, Metallomics 2020, 12(6) 868. "Hydrogen sulfide increases copper-dependent neurotoxicity via intracellular copper accumulation"
T. Ikawa, J. Sun, A. Takagi, S. Akai, J. Org. Chem. 2020, 85(5), 3383. "One-Pot Generation of Functionalized Benzynes from Readily Available 2‑Hydroxyphenylboronic Acids"
K. Okuda, B. G. M. Youssif, R. Sakai, T. Ueno, T. Sakai, T. Kadonosono, Y. Okabe, O. I. A. R. Salem, A. M. Hayallah, M. A. Hussein, S. Kizaka-Kondoh, H. Nagasawa, Heterocycles 2020, 101(2) 559. “Development of Near-infrared Fluorescent Probes with large Stokes shift for Non-Invasive Imaging of Tumor Hypoxia”
K. Oh-hashi, S. Matsumoto, T. Sakai, Y. Hirata, K. Okuda, H. Nagasawa, Appl. Biochem. Biotechnol. 2019, 188(4) 1009. “Effects of 2-(2-chlorophenyl)ethylbiguanide on ERAD component expression in HT-29 cells under a serum- and glucose-deprived condition”
H. Tsujino, T. Uno, T. Yamashita, M. Katsuda, K. Takada, T. Saiki, S. Maeda, A. Takagi, S. Masuda, Y. Kawano, K. Meguro, S. Akai, Bioorg. Med. Chem. Lett. 2019, 29(19) 126607. “Correlation of indoleamine-2,3-dioxigenase 1 inhibitory activity of 4,6-disubstituted indazole derivatives and their heme binding affinity”
K. Oh-hashi, S. Matsumoto, T. Sakai, Y. Nomura, K. Okuda, H. Nagasawa, Y. Hirata, Cell Biol. Toxicol. 2018, 34(4) 279. “Elucidating the rapid action of 2-(2-Chlorophenyl)ethylbiguanide on HT-29 cells under a serum- and glucose-deprived condition”
T. Ikawa, Y. Sumii, S. Masuda, D. Wang, Y. Emi, A. Takagi, S. Akai, Synlett 2018, 29(4), 530. “Synthesis of Optically Active 2,3-Disubstituted Indoline Derivatives via Cycloaddition Reactions between Benzynes and α,β-Unsaturated-γ-aminobutyronitriles”
M. Shimoji, H. Hara, T. Kamiya, K. Okuda, T. Adachi, Free Radical Res. 2017, 51(11–12), 978. “Hydrogen sulfide ameliorates zinc-induced cell death in neuroblastoma SH-SY5Y cells”
T. Hirayama, A. Mukaimine, K. Nishigaki, H. Tsuboi, S. Hirosawa, K. Okuda, M. Ebihara, H. Nagasawa, Dalton Trans. 2017, 46(46), 15991. “Bismuth-rhodamine: a new red light-excitable photosensitizer”
T. Hirayama, H. Tsuboi, M. Niwa, S. Kadota, A. Miki, K. Okuda, H. Nagasawa, Chem. Sci. 2017, 8(7), 4858. “A universal fluorogenic switch for Fe(II) ion based on N-oxide chemistry permits the visualization of intracellular redox equilibrium shift towards labile iron in hypoxic tumor cells”
S. Fukuda, K. Okuda, G. Kishino, S. Hoshi, I. Kawano, M. Fukuda, T. Yamashita, S. Beheregaray, M. Nagano, O. Ohneda, H. Nagasawa, T. Oshika, Graefes Arch. Clin. Exp. Ophthalmol. 2016, 254(12), 2373. “In vivo Retinal and Choroidal Hypoxia Imaging Using a Novel Activatable Hypoxia-Selective Near-Infrared Fluorescent Probe”
T. Ikawa, S. Masuda, A. Takagi, S. Akai, Chem. Sci. 2016, 7(8), 5206. “1,3- and 1,4-Benzdiyne equivalents for regioselective synthesis of polycyclic heterocycles”
K. Hattori, K. Koike, K. Okuda, T. Hirayama, M. Ebihara, M. Takenaka, H. Nagasawa, Org. Biomol. Chem. 2016, 14(6), 2090. “Solution-Phase Synthesis and Biological Evaluation of Triostin A and its Analogues”