ラジカル化合物の反応性制御と生体計測プローブ・治療化合物への展開

山﨑 俊栄 講師
令和4年度日本薬学会物理系薬学部会奨励賞 (2022年3月26日付)
タイトル:「ラジカル化合物の反応性制御と生体計測プローブ・治療化合物への展開」
DNA・脂質・タンパク質など生体分子のラジカル化の弊害
一般に、化合物は原子間で電子対を共有することで安定な共有結合を形成しています。ところが、ラジカルは、対をなしていない電子(不対電子)をもっているため、不安定で反応性が非常に高いことが知られています。生体内では、活性酸素が絶えず産生し、消去する機構が働いていますが、なにかのきっかけでこのバランスが崩れると、過剰に産生した活性酸素が生体成分であるDNAや脂質、たんぱく質などと反応し、次々にラジカル化してしまうことで、本来の生体機能が維持されず、病態が進行すると考えられています。そのため、生体内で産生するラジカルを検出することは、病態のメカニズム解明に向けて重要となります。また、ラジカルの細胞傷害性については、その傷害性をがん細胞に標的を向けることができれば、がん治療薬としての応用が期待されます。そこで、私は生体内で産生するラジカルの捕捉、あるいは細胞傷害性の高いラジカルの放出を実現する化合物開発を目的に、置換基効果を活用した化合物の物性制御の検討を進めてきました。これらの研究成果に対して、令和4年度日本薬学会物理系薬学部会奨励賞を受賞(2022年3月26日付)いたしました。
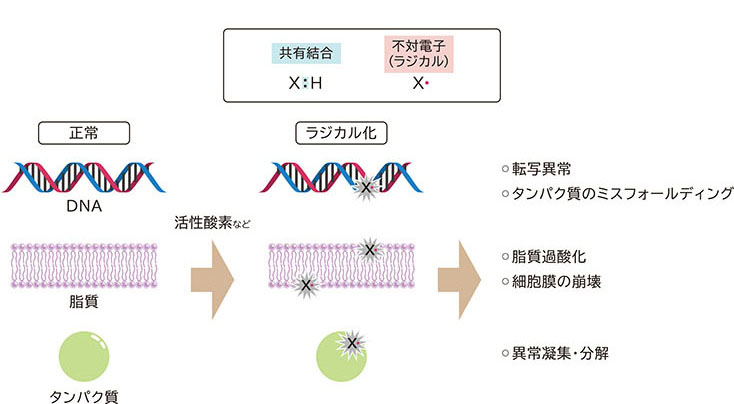
反応物性を制御した化合物開発とその応用に成功
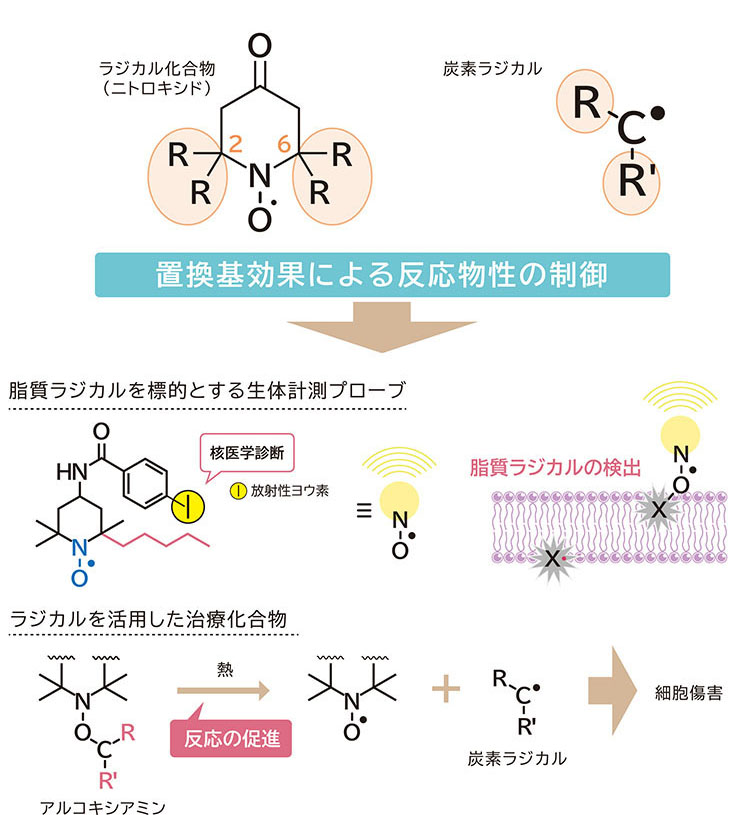
ラジカルの捕捉、放出を担う化合物として、ニトロキシドを用いて研究を進めました。ニトロキシドは窒素、酸素原子上に不対電子を有するラジカル化合物ですが、その周囲に嵩高い置換基を配しており、例外的に安定に存在することができます。その一方、炭素ラジカルとは鋭敏に反応し共有結合を形成することでアルコキシアミンを与えます。また、この逆反応は、生成物であるニトロキシドが熱力学的に安定に存在するため、エネルギー(熱)をかけることでラジカル開裂反応が進行します。これらの反応性は、ラジカル部分が反応の中心となっていることから、その周囲の置換基効果によって制御できると考えました。その結果、炭素ラジカルの捕捉選択性を向上させた化合物を開発し、さらには、生体検出を目的として放射性同位元素を標識した化合物の開発に成功しました。また、炭素ラジカルの放出による治療を目的として、生体pH条件下で活性化される化合物を開発し、培養細胞で高い傷害効果を示す化合物の開発に成功しました。今後も、標的に応じ最適な反応物性を示す化合物開発を進め、病態の進行機構の解明や治療薬の創出を進めていきたいと考えています。
同じカテゴリの研究レポート

-
ゲノム情報を利用したベンジルイソキノリンアルカロイド生合成系とその発現制御機構の解明、および物質生産への展開


-
コンドロイチン硫酸AはWnt3a/β-カテニン依存的なp53の発現亢進を介して骨芽細胞分化を抑制する


-
ワンポット立体選択的環化反応を基盤とする生物活性多官能複素環の実践的合成


-
免疫療法への応用を目指したプロバイオティクス由来細胞外小胞の有用性評価と機能改変技術の開発


-
がん固有の環境を標的とした癌治療増感をめざす創薬化学研究


-
コンドロイチン硫酸の硫酸化構造変化による骨硬化症の発症


-
高感度な免疫測定法の構築に必須な高親和力抗体を効率よく獲得する手法の開発


-
磁性リポソームを利用した標的組織内滞留型磁性化間葉系幹細胞の作製


-
亜鉛触媒反応を応用した細胞内亜鉛イオンの高感度検出プローブの開発


-
医薬品合成を指向した基質設計とカチオン性ヨウ素試薬を鍵とする複素環合成法の開発
